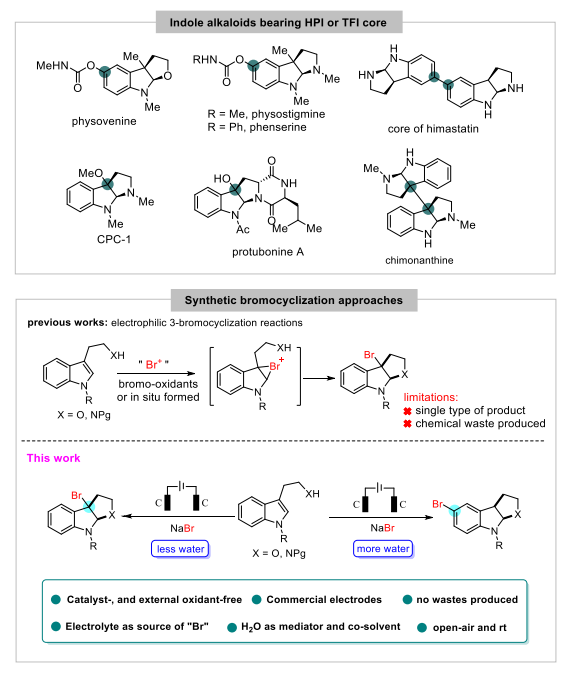
卤化(溴代)反应是有机合成中常用的化学反应,其产物能够有效、高选择性地发生化学转化,得到理想的目标分子。传统的溴化方法,往往需要使用过量的含溴有机氧化剂,从而会造成化学废物的大量产生。此外,亲电溴化反应位点在特定条件下主要依赖于底物反应位点的富电性,很难实现溴化反应的区域选择性调控。因此,发展新的、高效绿色的溴化反应新方法具有重要意义。近日,贵州省中国科学院天然产物化学重点实验室(贵州医科大学天然产物化学重点实验室)任海课题组利用可持续的电氧化策略,在无催化剂,无外加氧化剂的条件下,取得了水调控的溴化反应新进展。相关研究成果以“Water enables the tunable electrochemical synthesis of heterocyclic 3a- or 5a-bromoindolines”为题在线发表于国际化学领域著名期刊Green Chemistry (DOI:10.1039/D2GC02086F)。《Green Chemistry》是英国皇家化学学会旗下面向绿色化学领域的世界著名期刊,中科院化学大类一区,2022年影响因子为11.034。
吲哚啉核心结构广泛存在于天然产物和众多药用活性分子之中,其中3a-、5a-取代的吲哚啉是极具典型的两类分子骨架,如何实现该类结构衍生物的高效、绿色合成一直是有机化学和药物化学领域关注的热点。近年来,3-溴吲哚啉和5-溴吲哚啉作为合成该类分子的关键中间体得到了广泛的研究。传统的合成方法,色醇、色胺底物在NBS、NBAc、PyHBr3和DABCO溴盐等含溴氧化剂作用下,通过亲溴环化反应能够得到3-溴吲哚啉类化合物。但是,由于吲哚2,3-位固有的富电性,溴化反应只能选择性发生在吲哚的3位,且伴随有大量副产物的产生。高选择性地实现5-溴吲哚啉的直接构建具有非常大的挑战,一直未见报道。
本研究以廉价、绿色的溴化钠作为溴源,利用可持续的电氧化策略,通过改变反应体系中水的量成功实现了环化的3-溴吲哚啉和5-溴吲哚啉结构的高选择性合成。反应无需催化剂、外加的氧化剂,具有绿色环保、高效、高原子经济性等显著优点,并且建立的方法在复杂天然产物全合成及药物改造中具有重要应用前景。
上述研究工作得到了国家自然科学基金委,中国科学院西部之光,贵州省科学技术基金,贵州省千人创新创业人才项目和省部共建药用植物功效与利用国家重点实验室的支持。贵州医科大学药学院2020级硕士研究生吴英爱和王瑞安为本文的共同第一作者,吴伟副研究员,潘卫东研究员和任海副研究员为本文的通讯作者。
论文链接:https://pubs.rsc.org/en/content/articlelanding/2022/gc/d2gc02086f



